Albinismo oculocutaneo di tipo 2 (OCA2)
Initial posting: 27 Luglio 2009
last update
L’Albinismo Oculocutaneo di tipo 2 è associato al gene P (ora indicato come gene OCA2).Alla nascita, gli individui OCA2 (fig. 1) presentano capelli pigmentati, iride pigmentata e cute bianca. Il pigmento varia da una quantità minima ad una quantità quasi normale, riflettendo in parte, come in OCA1, il background etnico e familiare dell’individuo affetto, e si colloca in un ampio spettro, che, spesso, si sovrappone a quello presentato da OCA1B, OCA4, HPS e OA1, rendendo difficoltosa la diagnosi clinica. “I capelli pigmentati alla nascita”, leggermente pigmentati, di un giallo/biondo chiaro, o più pigmentati, di un biondo definito o biondo dorato o anche rosso, salvo eccezioni (neonati con capelli bianchi, come in OCA1), è il carattere che aiuta a distinguere tra OCA1 e OCA2 (king, 2003). Tenendo presente, però, l’esiguità, se non l’assenza di capelli in molti neonati, la difficoltà nel distinguere il capello bianco dal capello giallo/biondo chiaro (se non su di un fondo scuro) e il normale ritardo nello sviluppo del sistema pigmentario nei bambini del nord Europa, è difficile distinguere OCA2 da OCA1 nei primi mesi di vita. Nel corso del tempo, i capelli possono diventare più scuri (in modo meno pronunciato che in OCA1B), ma molti individui conservano lo stesso colore di capelli per tutta la vita. La cute è bianca, ma mai così bianca come in OCA1A, perché i melanociti sintetizzano una certa quantità di melanina, rappresentata, per lo più, da feomelanina gialla piuttosto che da eumelanina marrone-nera. Non presenta pigmentazione generalizzata, bensì localizzata (nei, efelidi e lentiggini) in aree esposte al sole, e di solito non si abbronza. L’iride è di un colore blu-grigio o di un pigmento chiaro (nocciola/castano chiaro), con un grado di trasparenza, alla transilluminazione del globo oculare, correlato alla quantità di pigmento presente.Il classico fenotipo “OCA tirosinasi-positivo” (OCA ty-pos), è il fenotipo OCA2 più comunemente riscontrato tra gli Africani e gli Afro-Americani. I capelli sono gialli e rimangono tali per tutta la vita; possono diventare più chiari con l’invecchiamento, probabilmente come normale ingrigimento legato all’età. La cute, bianco crema alla nascita, cambia poco nel corso del tempo, non presenta pigmentazione generalizzata, ma localizzata ( nei, efelidi e lentiggini) solo in alcuni individui, e di solito non si abbronza. L’ride è blu-grigia o di un pigmento chiaro (di solito nocciola o castano chiaro).Il fenotipo OCA Brown (BOCA), considerato in passato come un tipo di OCA, risulta attualmente, in seguito a dati forniti da analisi molecolare, una variante fenotipica di OCA2. I primi casi sono stati riscontrati nelle popolazioni Africane ed Afro-Americane. Alla nascita i capelli e la cute sono di un colore castano chiaro e l’iride è grigia. Con il tempo il colore della cute cambia poco, ma può scurirsi in seguito ad esposizione al sole. I capelli possono diventare più scuri. L’iride può accumulare più pigmento marrone chiaro e presenta una trasparenza punteggiata e radiale. Il pigmento retinico è moderato. L’acuità visiva è tra 20/60 e 20/150. Gli individui con OCA Brown provenienti dalle popolazioni del Nord Europa e dell’ Asia, con le caratteristiche oculari dell’Albinismo, possono presentare una pigmentazione cutanea quasi normale e apparire ipopigmentati solo quando confrontati con gli altri membri della famiglia.Un ampio spettro fenotipico pigmentario intermedio si pone tra il classico fenotipo OCA ty-pos e il fenotipo BOCA,Molti casi un tempo indicati come AROA e OA1, con coinvolgimento cutaneo scarso o per nulla evidente, rientrano ora nello spettro fenotipico di OCA2.Il gene P è l’unico gene associato ad OCA2.E’ localizzato sul cromosoma 15q11.2-q12, regione associata con la sindrome di Prader-Willi (PWS) e la Sindrome di Angelman (AS). L’omologo murino, il gene p, è localizzato sul cromosoma 7, regione di omologia sintenica con la regione 15q umana.Contiene 24 esoni che codificano una proteina integrale della membrana melanosomale di 838 aa e di 110 KDa, la proteina P (fig. 2), con 12 domini transmembrana. La sua funzione precisa è sconosciuta. Studi, finora svolti, supportano l’ipotesi che abbia un ruolo, come trasportatore, nella regolazione del pH melanosomale (). Somiglianze strutturali sono state rilevate tra la proteina P e la proteina antiporto H+/Na+ di E. coli.
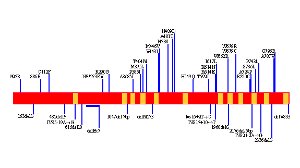
Fig. 2. Struttura della proteina P e localizzazione delle mutazioni nel gene P umano, associate ad OCA2. Slide
In rosso, la regione codificante del gene P. In giallo, le 12 regioni transmembrana della proteina P. In alto, la localizzazione delle mutazioni missenso.In basso, la localizzazione delle mutazioni nonsenso, frameshift e splice site. La linea blu orizzontale indica la delezione di 2,7 Kb che elimina l’esone 7 (54 aa) del gene P, determinando la formazione di un codone di stop prematuro.
Da King, The clinical spectrum of Albinism in human. ( Lista completa delle mutazioni all’indirizzo http://albinismdb.med.umn.edu/oca2mut.html)
Sono state riportate più di 50 mutazioni P (fig. 2), tutte associate al fenotipo OCA2. La mutazione più comune del gene P è una delezione di 2,7 kb, che comprende l’intera sequenza codificante dell’esone 7 e le sequenze introniche fiancheggianti (2.7-kb del, ex7del) e si riscontra con alta frequenza nelle popolazioni Africane ed Afro-Americane. Studi condotti da Stevens (1997) e da Aquaron (2007) confermano l’origine africana di questa mutazione. L’analisi dell’aplotipo delle popolazioni Africane, in particolare dell’Africa Centrale e Meridionale, suggerisce che la delezione sia comparsa una sola volta, prima della divergenza di queste popolazioni, circa 2000-3000 anni fa. L’insolita alta frequenza delle mutazioni OCA2, ed in particolare di questa delezione, suggerisce una selezione o una deriva genetica. Le altre mutazioni riportate sono mutazioni missenso, mutazioni frameshift, mutazioni splice-site e delezioni inframe.
Le mutazioni missenso, a differenza di quelle del gene TYR, non sono raggruppate in regioni definite, anche se la maggior parte di esse si ritrova nella metà carbossiterminale della proteina, che contiene la maggior parte dei domini transmembrana (tra o al confine dei TMs).
La mutazione missenso “p.Val443Ile” è la mutazione P più comune nelle popolazioni del Nord Europa.
La maggior parte degli individui OCA2 è eterozigote composta e in circa la metà degli individui OCA2 non Africani, riportati in letteratura, è stata individuata solo una delle 2 mutazioni.
L’alta frequenza di varianti di significato ignoto (polimorfismi o mutazioni?) riscontrata nel gene P, la scarsità di dati relativi ad analisi di sequenza in individui OCA2 ed in individui di controllo e la difficile analisi funzionale del prodotto genico, riducono l’utilità del test genetico per la diagnosi di OCA2. Rendono inoltre difficile qualsiasi relazione genotipo-fenotipo, per cui non è possibile prevedere con alcun grado di certezza la pigmentazione cutanea, la pigmentazione oculare e lo sviluppo oculare risultanti da una determinata mutazione del gene P.
Da tener presente che molte varianti del gene P, insieme alle varianti del gene MCIR, hanno un effetto predominante sul normale controllo multigenico del colore della cute, dei capelli e degli occhi.
Il meccanismo mediante il quale un difetto nella proteina P determina riduzione/assenza dell’attività tirosinasica è in corso di studio. Sembra che i melanoctiti-p immortalizzati, a differenza dei melanociti selvatici, secernino vescicole scure, contenenti tirosinasi ed una piccola quantità della proteina TYRPI, nel mezzo di coltura. Queste vescicole di secrezione provenienti dalla rete transgolgiana cambierebbero percorso, dirigendosi verso la membrana plasmatica melanocitica e non verso i melanosomi secondari (stadio II). Tale percorso anomalo è riscontrato anche nei melanociti primari underwhite . Questo farebbe pensare ad un ruolo di regolatori del traffico intracellulare degli enzimi melanogenici da parte di due proteine melanosomali (P e MATP), con la topologia di trasportatori membranali (da Costin, 2003: Toyofuku, 2002).
BIBLIOGRAFIA
Aquaron, R.; Soufir, N.; Berge-Lefranc, J.-l; Badens, C.; Austerliz, F.; Grandchamp, B.. Oculocutaneous Albinism type 2 (OCA2) with homozygous 2,7 kb deletion of the P gene and sickle cell disease in a Cameroonian family. Identification of a common TAG haplotype in the mutated P gene. J. Hum. Genet. 52: 771-780. 2007.
Costin GE, Valencia JC, Vieira WD, Lamoreux ML, Hearing VJ. Tyrosinsase processing intracellular trafficking is distrupted in mouse primary melanocytes carrying the Underwhite (uw) mutation. A model for oculocutaneous albinism (OCA) type4. J Cell Sci; 116: 3203-12. 2003. Text
King R. A., Pietsch J., Fryer J. P., Savage S., Brott M. J., Russel-Eggitt I., Summers C. G., Oetting W.S. Tyrosinase gene mutations in oculocutaneous albinism 1 )OCA1): definition of the phenotype. Hum. Genet. 113: 502-513. 2003. Text
Stevens, G.; Ramsay, M.; Jenkins, T. Oculocutaneous albinism (OCA2) in sub-Saharan Africa: distribution of the common 2.7-kb P gene deletion mutation. Hum. Genet. 99: 523-527, 1997.
Toyofuku K, Valencia JC, Kushimoto T, Costin GE, Virador VM, Vieira WD, Ferrans VJ, Hearing VJ. The etiology of oculocutaneous albinism (OCA) type II: the pink protein modulates the processing and transport of tyrosinase. Pigment Cell Res. 2002; 15: 217–24.
Yuasa, I.;Umetsu, K.; Harihara, S.; Miyoshi, A.; Saitou, N.; Park, K. S.; Dashnyam, B.; Jin, B.; Lucotte, G.; Chattopadhyay, P. K.; Henke, L.; Henke, J. OCA2*481Thr, a hypofunctional allele in pigmentation, is characteristic of northeastern Asian populations. J. Hum. Genet. 52: 690-693.2007


